Proteini za podmlađivanje mozga

Feritinske bjelančevine se s godinama postupno gomilaju u mozgu, guše memoriju i usporavaju učenje. Njihovo blokiranje vraća mladenačku svježinu mozgu ostarjelih miševa, nagovještajući potencijalne terapijske perspektive
Starenje mozga se obično opisuje kao neizbježan i linearan proces: svaki dan odumre i zauvijek nestane par (stotina / tisuća) sinapsi, neuroni postaju sve tromiji i trošniji, a nekada bistar i svjež slijed misli sve više podsjeća loše zakrpanu ostarjelu odjeću: rupa ovdje, rupa ondje... sve dok „glava više ne radi kao nekad“.
S druge strane, neuroznanost se zadnjih desetljeća uporno trudi pronaći trikove i hackove kojima bi se starenje mozga moglo ublažiti, usporiti, pa i – u idealnom scenariju – posve zaustaviti. Najnovije otkriće iz laboratorija Sveučilišta San Francisco u Kaliforniji novi je kamenčić u mozaiku tih nastojanja: čini se da neurološko starenje nije samo pitanje istrošenih živčanih stanica, nego i „kemijskih sabotera“, metaboličkih produkata koji se s godinama počnu nakupljati u mozgu i „guše“ njegovu normalnu funkcionalnost. Slijedom logike, ako bi se te sabotere moglo onesposobiti, mozak bi povratio svoju mladenačku žustrost.
Više od „pohabanosti“
U popularnoj predodžbi mozak se starenjem ponaša poput dotrajalog računala: memorija sporije radi, procesor šteka, a neki kablovi povremeno izgube kontakt. No u biologiji takva metafora ne drži vodu. Mozak nije stroj, nego živi ekosustav u kojem neuroni i pomoćne glijalne stanice neprestano komuniciraju, umnožavaju se i reorganiziraju. Starenje mozga ne znači samo da se stanice troše, nego i da se remeti ravnoteža u tom ekosustavu. Neke molekule koje u mladosti služe kao korisni regulatori u starosti počinju djelovati destruktivno.
Upravo takav primjer je jedan naizgled neugledan protein, nazvan ferritin light chain 1 (FTL1). Njegova uloga u normalnim okolnostima nije dramatična – radi se o proteinu koji veže željezo i pomaže održavati taj visokooksidativni metal u mozgu pod kontrolom. No kako mozak stari, FTL1 se počinje gomilati u hipokampusu, regiji odgovornoj za učenje i pamćenje, i na kraju djeluje poput korova u zapuštenom vrtu: zakrči fine spojeve među neuronima, guši prijenos informacija i smanjuje kapacitet mozga. Kad su znanstvenici genetskim inženjeringom snizili razinu FTL1 u mozgu ostarjelih miševa, dogodilo se nešto nalik biokemijskom botoksu za sinapse – sinapse su se počele obnavljati, a životinje su opet učile i pamtile gotovo jednako dobro kao njihovi mladi rođaci.
Vraćanje mladosti
Do sada su najčešće mete znanstvenika bile beta-amiloid i tau protein, proteini povezani s Alzheimerovom bolešću. No oni su tipični za demenciju kakva nastaje u patološkim stanjima; s druge strane – običan, svakodnevni pad kognitivnih sposobnosti nije nužno vezan uz takve ekstremne, patološke naslage. Istraživanje FTL1 ukazuje na mogućnost da iza „normalnog“ starenja stoje drugi, suptilniji mehanizmi nego oni kakve viđamo u Alzheimerovoj demenciji. Ako se ti mehanizmi razotkriju i nauče kontrolirati, možda se jednog dana kognitivni pad neće smatrati nužnim pratiocem starosti.
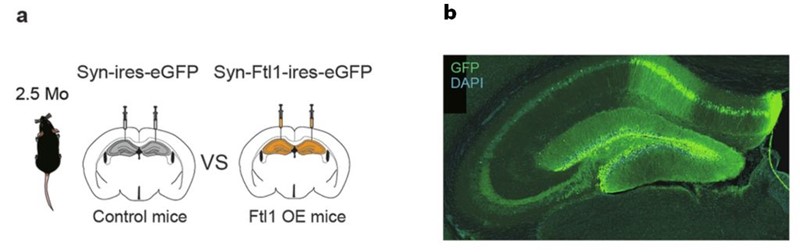
U studiji objavljenoj u časopisu Nature Aging (onoj iz već spomenutog laboratorija u San Franciscu) znanstvenici su proučavali razine FTL1 u mozgovima mladih i starih miševa. Rezultati su bili jasni: što je životinja bila starija, to se više FTL1-a nalazilo u hipokampusu. Zatim su pomoću genetskog uređivanja i ciljane terapije smanjili razine tog proteina – i rezultat je bio impresivan: stare životinje su na testovima labirinta i zadataka memoriranja pokazivale performanse koje se gotovo nisu razlikovale od mladih. Mikroskopskom analizom sinapsi potvrđeno je da su se veze među neuronima ponovno počele obnavljati.
Ono što je posebno zanimljivo jest da se pozitivni učinak pojavio ubrzo nakon navedene genetske intervencije i terapije, što sugerira da stanice zagušene FTL1 nisu zauvijek izgubljene, nego ih je samo potrebno osloboditi neželjenog pritiska koji ih blokira. Drugim riječima, mozak starog miša nije bio nepovratno oštećen – bio je samo „zatrpan otpadom“.
Vidi što su im uradili sa mozgom, mama!
Kako bi istraživanje bilo uvjerljivije, znanstvenici su osmislili čitav niz intervencija u mozgu miševa. U prvoj varijanti (slika 1) uzeli su mlade životinje i virusnim putem pojačali aktivnost FTL1 proteina u hipokampusu. Rezultat je bio ubrzano starenje – mladi mozgovi počeli su se ponašati kao stari, s narušenim sinapsama i slabijom memorijom.
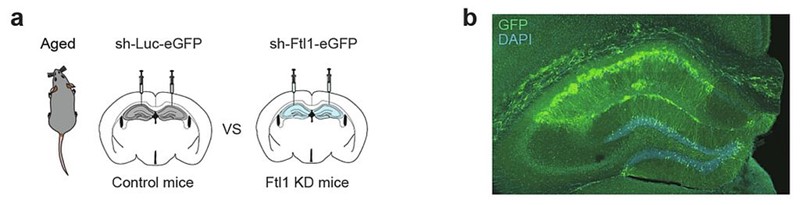
Zatim su napravili suprotan eksperiment na starim životinjama (slika 2): tamo su FTL1 utišali, koristeći shRNA tehnologiju za njegovo djelomično blokiranje (takozvani knockdown). Odjednom, sinaptičke veze i kognitivne funkcije ostarjelih mozgova počele su se popravljati, gotovo kao da se radilo o povratku u mlađu dob.
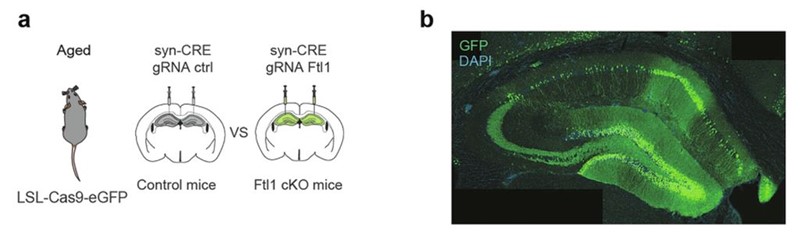
Konačno, otišli su i korak dalje (slika 3). U starim miševima primijenili su CRISPR-Cas9 sustav kojim su ciljano isključili gen za FTL1 u neuronima hipokampusa. Takvo potpuno blokiranje (tzv. knockout) pokazalo je najjasnije: kad se FTL1 sasvim izbriše iz jednadžbe, mozak starih miševa pokazuje snažne znakove obnove sinapsi i bolju izvedbu na testovima pamćenja.
Drugim riječima, serija pokusa na tri načina – od pojačavanja, preko utišavanja do potpunog isključivanja gena – dala je konzistentnu sliku: FTL1 je ključni igrač u starenju mozga, a time i mogući cilj koji otvara prostor za potencijalne terapije.
Zašto baš željezo?
Jedno od temeljnih i najviše intrigantnih pitanja jest: zašto se FTL1 uopće gomila s godinama? Već dugo se zna da metabolizam željeza pokazuje povezanost s neurodegeneracijom, propadanjem moždanog tkiva. Previše željeza u mozgu može potaknuti oksidativni stres i oštećenje neurona. Kod Parkinsonove bolesti, primjerice, višak željeza u dijelu mozga zvanom substantia nigra smatra se važnim čimbenikom nastanka simptoma. Čini se da priroda koristi željezo kao dvostruko sječivo oružje: potrebno je za normalan rad, ali vrlo lako postaje toksično ukoliko se ne obuzdava njegova visoka sklonost vezivanju kisika i posljedičnom oksidacijskom stresu za stanice.
Povećana količina proteina FTL1 u starijoj dobi možda predstavlja pokušaj mozga da kontrolira željezo, ali u tom procesu se stvara više štete nego koristi. Drugim riječima, ono što je u mladosti bila zaštitna mreža, u starosti se pretvara u okove. Ovo je u biologiji poznat fenomen: molekule i procesi koji pomažu mladom organizmu da preživi često postaju kontraproduktivni kad tijelo ostari. Otklanjanje takvih „blokirajućih“ molekula i procesa u nekim tkivima uspješno vraća svježinu i funkcionalnost.
Od miševa do ljudi je dug i trnovit put
Premda otklanjanje suvišnog FTL1 zvuči kao recept za eliksir moždane mladosti, valja istaknuti kako za sada sve navedeno vrijedi samo za – miševe. Ljudski mozak je daleko složeniji, mehanizmi regulacije željeza i proteina su u nekim nijansama i metaboličkim putevima drukčiji nego u mišjim mozgovima, a znanstvenici još nisu započeli pokuse na „ljudskom materijalu“, pa još uvijek ne znamo je li FTL1 jednako problematičan u ljudskim neuronima, niti kakve bi nuspojave moglo imati njegovo blokiranje.
Željezo je, naime, ključno za rad različitih tipova stanica i tkiva (ne samo moždanih), a feritinski proteini poput FTL1 paze kako ne bi postalo toksično. Igranje s tim sustavom zahtijeva finu ravnotežu, jer pogrešnim doziranjem terapije i blokade riskiramo ozbiljne poremećaje metabolizma – i to ne samo u mozgu.
Osim toga, istraživački put od miševa do čovjeka uključuje brojne prepreke: od pronalaska sigurnih inhibitora, preko složenijih i skupljih kliničkih ispitivanja, sve do legislativnih i etičkih pitanja. No upravo zato ovakva otkrića izazivaju interes i uzbuđenje – ne zato što sutra možemo očekivati tabletu protiv zaboravljivosti, nego zato što otvaraju potpuno novo polje istraživanja.
Glija i glimfatsko „čišćenje mozga“
FTL1 priča uklapa se u širi val istraživanja koji gledaju na starenje mozga kao na poremećaj ravnoteže, a ne samo kao istrošenost. Primjerice, glijalne stanice, koje neurone hrane i štite te ih održavaju na životu, s godinama postaju previše aktivne i počnu proizvoditi spojeve koji su medijatori kronične upale i koji štete sinapsama. Drugi primjer je glimfatski (glija + limfa) sustav – mreža kanalića koja tijekom spavanja „ispire metabolički otpad“ iz mozga. Kod starijih ljudi taj sustav radi sve lošije, pa se metabolički nusprodukti gomilaju i oštećuju stanice.
U istom duhu, isticanje uloge FTL1 u opadanju sposobnosti pamćenja i moždane funkcionalnosti ne znači da je on jedini krivac. Vjerojatno je riječ o kombinaciji velikog broja faktora – ali svaki novi trag pomaže sastaviti slagalicu. Ako u jednom slučaju možemo blokirati upalne molekule, u drugom poboljšati glimfatsko čišćenje, a u trećem smanjiti FTL1, možda jednog dana dobijemo koktel terapija koje će uvelike usporiti ili čak preokrenuti kognitivno starenje.
Ako se pokaže da je moguće znatno usporiti ili čak vratiti memorijske sposobnosti starijih ljudi, implikacije su goleme. U svijetu u kojem populacija stari, demencija i kognitivni pad postaju jedan od najvećih javnozdravstvenih izazova. Trenutačno ne postoji nijedan lijek koji spektakularno vraća memoriju – postoje samo skromno učinkovite terapije koje u nekoj mjeri usporavaju propadanje.
Učenje starog psa novim trikovima
Zamisliti budućnost u kojoj se sedamdesetogodišnjaci ponovno sjećaju novih imena i uče nove vještine jednako lako kao i tridesetogodišnjaci znači zamisliti i drugačiju ekonomiju, obrazovanje i radnu dinamiku u kojima se kombiniraju iskustvo sa svježinom i kapacitetom.
Naravno, ne treba odmah zamišljati „super-starce“ koji u 90. godini života s lakoćom uče programiranje u Assemblyju i konkuriraju tridesetogodišnjacima za stipendije na postdoktorskim studijima raketnog inženjerstva. Ali već i blago pomlađivanje moždanih funkcija imalo bi ogroman učinak na kvalitetu života i na smanjenje troškova zdravstvene skrbi.
Kako to obično biva s uzbudljivim otkrićima, valja se oduprijeti iskušenju da sve odmah prenesemo u sfere „čarobnog lijeka“. Povijest medicine puna je molekula koje su u miševima izgledale obećavajuće, a u ljudima potpuno podbacile. Uz to, ljudsko starenje je dug i složen proces, s genetskim, okolišnim i životnim čimbenicima. FTL1 je možda važan komad slagalice, ali nije cijela slika.
Oprezni entuzijazam
Znanstvenici naglašavaju da je ovo tek prvi korak. Potrebna su daljnja istraživanja da se potvrdi njegova uloga u ljudskom mozgu, pronađu sigurni načini moduliranja i ispitaju dugoročne posljedice. Tek tada se može razmišljati o kliničkim ispitivanjima.
Otkriće da protein FTL1 može blokirati sinapse i time ubrzati starenje mozga mijenja način na koji gledamo kognitivni pad koji prate životnu dob. Umjesto neizbježne sudbine, mozak se pokazuje kao sustav koji se može „otkočiti“. Ako se rezultati potvrde i kod ljudi, pred nama je uzbudljivo doba istraživanja – ne eliksira besmrtnosti, ali možda eliksira bistrine. I to je već dovoljno da se starost dočeka s nešto manje straha i nešto više nade.
Za sada, jedino što možemo jest nastaviti učiti i vježbati mozak – jer neuroplastičnost je stvarna i redovito treniran mozak otporniji je na starenje. A u budućnosti, možda ćemo za očuvanje mentalne svježine uz sudoku i križaljke imati i biokemijsku pomoć.
Tko zna, možda se sve to jednog dana i ostvari, pa bi farmaceutska industrija mogla uvesti novu kategoriju: lijekovi protiv zaboravnosti. U ordinaciji obiteljskog liječnika pacijent će umjesto: „Imate li Viagru?“ pitati: „Imate li nešto da se sjetim zašto uzimam Viagru?“... a liječnik će uzdahnuti i reći: „Evo vam recept za FTL1-blokator, ali nemojte ga miješati s alkoholom, jer posljedice mogu biti nesagledive.“

Igor „Doc“ Berecki je pedijatar-intenzivist na Odjelu intenzivnog liječenja djece Klinike za pedijatriju KBC Osijek. Pobornik teorijske i praktične primjene medicine i znanosti temeljene na dokazima, opušta se upitno ne-stresnim aktivnostima: od pisanja znanstveno-popularnih tekstova u tiskanom i online-izdanju časopisâ BUG, crtkanja računalnih i old-school grafika i dizajna, zbrinjavanja pasa i mačaka, fejsbučkog blogiranja o životnim neistinama i medicinskim istinama, sve do kuhanja upitno probavljivih craft-piva i sasvim probavljivih jela, te neprobavljivog sviranja bluesa.
















