Dolazi novo ugljeno doba
Svaki se organski spoj, tako se uči u školi, može pretvoriti u ugljik. No kako napraviti elektronički sklop od tankog sloja ugljika drugo je pitanje – i nov izazov kemiji i nanotehnologiji.

Je li ugljik (ugljen) najstariji materijal što ga poznaje čovjek teško je reći. Pa ipak, nema sumnje da je ugljen bio prvi kemijski proizvod što ga je čovjek napravio nakon što je otkrio vatru: o tome svjedoče slike na spiljskim zidovima nacrtane upravo ugljenom (taj se crni pigment i danas koristi u tiskarstvu), a još više vrhovi kopalja i strelica ojačani karbonizacijom – istim postupkom što ga i danas koriste vinogradari za obradu kolja.
I tako je počela povijest ugljena – koja traje i traje. Drveni ugljen se prvo koristio u metalurgiji, za istaljivanje metala i kao gorivo za kovačka ognjišta, onda je došao mineralni, kameni ugljen koji je pokrenuo industrijsku revoluciju: parni stroj, željeznica, parobrod... Došlo je doba ugljena i čelika, doba kada se privredna (i vojna!) snaga zemlje mjerila tonama iskopanog ugljena i proizvedenog čelika.

No ta su doba iza nas. Ugljen, i njegova malo nježnija sestra nafta, dobili su epitet uništavatelja planeta, glavnih krivaca za globalno zatopljenje. Treba potpuno izbaciti fosilna goriva, kažu, da bismo spasili planet. Točno. No to ne znači da treba posve zabraniti ugljen i naftu. Baš naprotiv. Treba ih pretvoriti u sirovine za nove materijale, nove proizvode kemijske industrije. No koji je materijal najpogodniji sa stajališta niskougljične ekonomije? PVC sadrži, primjerice, isto toliko klora (48 %) koliko i ugljika (i samo 4 % vodika). No, ima jedan materijal koji sadrži 100 % ugljika. Taj materijal se materijal zove ugljen, ili bolje rečeno ugljik u svojim bezbrojnim alotropskim modifikacijama.
Kažem „bezbrojnim“ premda se sve donedavno u školi učilo kako ugljik ima samo dvije modifikacije, grafit i dijamant. To je točno, jer se samo te dvije modifikacije pojavljuju u prirodi, kao minerali. No onda je krajem prošlog stoljeća došla revolucija: otkriven je buckminsterfulleren, „najljepša“ (najsimetričnija) molekula na svijetu, potom drugi fullereni, pa grafeni i nanocjevćice. Ugljična vlakna postala su materijal za izradu zrakoplova (aviona, helikoptera i cepelina) i sportskih automobila. Ugljik ponovno stupa na scenu, ali ne kao gorivo nego u obliku novih materijala zahvaljujući tehnologijama utemeljenima na oplemenjivanju organskih spojeva, dakle spojeva koji se po definiciji mogu pretvoriti u ugljen, u ugljik (karbogeni spojevi).
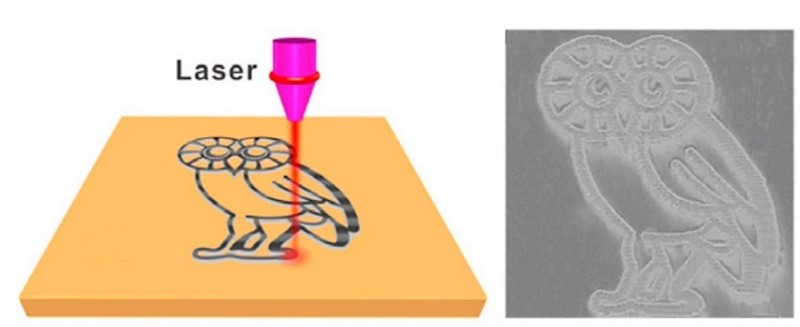
Karbonizacija u pećima prepustila je svoje mjesto karbonizaciji upotrebom lasera. Laserska zraka, posebice zraka infracrvenog lasera, usmjerena na bilo koji organski materijal pretvorit će ga u ugljen, no pitanje svih pitanja je kakav ugljen.
Kvaliteta ugljena ne ovisi samo o laserskoj zraci (snazi, vremenu ozračenja) nego i o polaznom materijalu, koji se zove, jednostavno, HCM (heavy carbonaceuous material). To dvoje mora biti dobro usklađeno da bi se dobilo što se želi, a to nešto je tanki film grafena ili grafenovog oksida na polaznom materijalu, a on može biti polimerna folija, tekstil, drvo, pa čak i kruh (pečenje tosta laserom!). Ono što se na kraju dobiva je tanak sloj ugljena koji može za sve i svašta poslužiti (npr. za pisanje oznaka), no najvažnija mu je primjena u elektronici.
Grafit, grafen, ugljik općenito vodi električnu struju. To posebice vrijedi za grafen čija specifična električna vodljivost iznosi 108 S/m (naravno ako je posve čist i bez defekata u strukturi) – što je više od vodljivosti bakra (5·107 S/m). Kako se laserska zraka može usmjeriti na vrlo male površine, jasna je i primjena: tom se tehnologijom mogu izrađivati elektronički sklopovi od svakog materija i na svakom materijalu – uz uvjet, naravno, da sadrži ugljik – pa i na suhom kruhu ako hoćete.

No iza svega toga, iza svih tih napora i rezultata mnogih znanstvenika koji su predočeni u podužem preglednom radu objavljenom ovog mjeseca u časopisu Matter, leži jedan veliki ali. Taj „ali“ proizlazi iz same naravi kemijske reakcije. Reakcija karbonizacije izrazito je kaotična, pa je teško predvidjeti što će na kraju ispasti. Ovisno o tehnološkom postupku dobivaju se specifične vodljivosti od 102 do 104 S/m, a to je jako, jako daleko od vodljivosti čistog grafena, 108 S/m. Da bi riješili problem, znanstvenici su u pomoć pozvali teoriju, pa provode računalne simulacije kako bi smanjili omjer vodika prema ugljiku (H:C) i povećali udio sp2 hibridiziranih ugljikovih atoma – ili, jednostavno rečeno, da bi dobili materijal što sličniji grafenu. Tehnologija kamenog doba, no na način 21. stoljeća, daleko je od svake jednostavnosti.

Nenad Raos je kemičar, doktor prirodnih znanosti i znanstveni savjetnik u trajnome zvanju, sada u mirovini. Autor je i koautor više od stotinu znanstvenih i stručnih radova iz područja bioanorganske i teorijske kemije, molekularnog modeliranja te povijesti kemije i komunikacijskih vještina u znanosti. Još od studentskih dana bavi se popularizacijom znanosti. Sada piše za Čovjek i svemir te, naravno, Bug online. Sedam je godina bio glavni i tehnički urednik časopisa Priroda, a danas je urednik mrežne stranice Panopticum. Koautor je dva sveučilišna udžbenika i autor 13 znanstveno-popularnih knjiga. Nagrađen je Državnom godišnjom nagradom za promidžbu i popularizaciju znanosti 2003. godine.















