15 metala u jednoj kovini
Ne miješaju se svi metali lako, neki baš nikako, no zahvaljujući novom postupku, „visokoentropijskom dizajnu“ moguće je – kako se čini – napraviti slitinu praktički od bilo koje kombinacije metala

Alkemičari su sanjali o tome da naprave – uz kamen mudraca koji bi ujedno bio eliksir, lijek za sve bolesti – i leguru od sedam metala. Kojih metala? Pa naravno, svih tada poznatih metala, a to su zlato, srebro, živa, bakar, željezo, kositar i olovo. Ne samo da bi time svih sedam metala pretvorili u jedan, nego bi svoju čudesnu kovinu na čudesan način povezali sa svemirom, sa zvijezdama. Još od antičkih vremena vjerovalo se naime u mističnu vezu sedam metala sa sedam planeta: zlato – Sunce, srebro – Mjesec, živa – Merkur, bakar – Venera, željezo – Mars, Jupiter – kositar i Saturn – olovo. (Tu treba napomenuti da riječ „planet“ nema veze s heliocentričnim sustavom: planet izvorno znači „zvijezda lutalica“, to je nebesko tijelo koje danju ili noću putuje po nebeskom svodu.) No metali se ne miješaju lako. Neki se uopće ne miješaju, poput žive i željeza. Zato kao iznenađenje dolazi vijest da su američki i kineski znanstvenici uspjeli prirediti stabilnu, monofaznu leguru koja se sastoji od čak 15 metala. Kako su to postigli?
Kada sam pročitao njihov rad „Extreme mixing in nanoscale transition metal alloys (Ekstremno miješanje u slitinama prijelaznih metala nanometarskih dimenzija)" objavljen u časopisu Matter, odmah sam pomislio na Kolumbovo jaje. Tajna njihove revolucionarne metode posve je jednostavna: povišenje temperature.
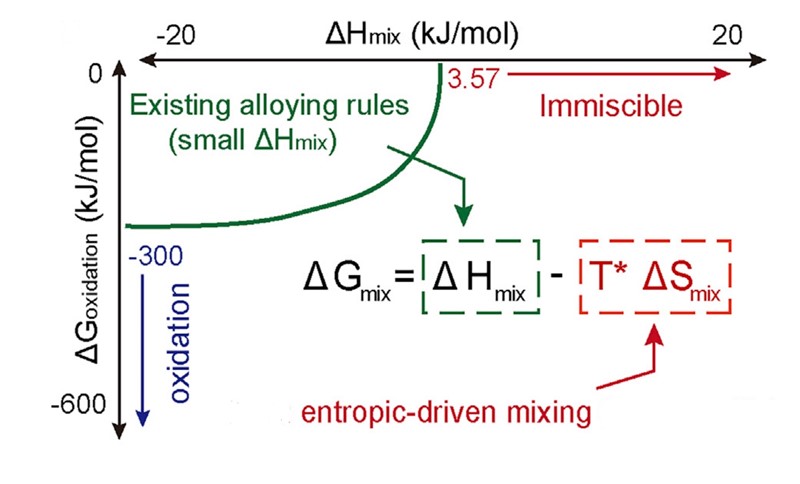
Da bi se shvatilo u čemu je riječ, treba razumjeti malo termodinamike, ili – bolje rečeno – treba početi od osnovne jednadžbe za svaku kemijsku, pa i fizičku promjenu: ΔG = ΔH – TΔS (G je Gibbsova slobodna energija, H je toplina, entalpija, S entropija, a T apsolutna temperatura). U slučaju pripreme legura ta se jednadžba piše kao ΔGmix = ΔHmix – T*ΔSmix, gdje „mix“ označava, jasno je, proces miješanja. Da bi se metali mogli miješati, tj. stvoriti leguru, ΔHmix mora biti što manja (ΔHmix < 3,57 kJ/mol) dok za Gibbsovu energiju vrijedi sličan uvjet ΔGmix > -300 kJ/mol, no zbog drugog razloga. Kod nižih vrijednosti Gibbsove energije metali se ne mogu izlučiti (reducirati) ugljikom iz svojih spojeva. Na vrijednosti ΔHmix i ΔSmix ne može se utjecati jer one ovise o komponentama koje čine smjesu, no može se posredno utjecati na član -T*ΔSmix promjenom temperature stvaranja, T*. I upravo su to učinili autori spomenutog rada u vrlo jednostavnom pokusu. Ugljičnu nit nanometarske debljine natopili su solima metala od kojih su kanili načiniti slitinu, a zatim su nit zagrijali protokom struje na temparaturu od 1.800 K (oko 1.600 oC). Na ugljikovoj niti došlo je do redukcije soli uz stvaranje nanočestica od „nemogućih legura“. Najveći uspjeh bila je već spomenuta legura 15 metala, od toga 14 prijelaznih (15-HEA, HEA = high-entropy alloy): PtPdRhRuIrAuCuFeCoNiCrMnWMoSn.
U leguri je došlo do stvaranja nemogućih kombinacija, poput zlata s volframom (Au-W) i molibdenom (Au-Mo). Entropijski je član, -T*ΔSmix, pao na vrijednost od oko -40 kJ/mol, čime se ΔGmix spustio ispod graničnih -300 kJ/mol, no to nije smetalo budući da je pri toj temperaturi, 1.800 K, Gibbsova energija za redukciju metala ugljikom iznosi oko -500 kJ/mol.

No ako se iz ovih termodinamičkih visina spustimo na zemlju, u područje strukturne kemije, otkriva se čudo miješanja 15 metala. Za legure vrijedi isto pravilo kao i za svaku drugu smjesu: slično se miješa sa sličnim. Taj „zahtjev sličnosti“ u slučaju smjesa metala našao je izraz u Hume-Rotheryjevom pravilu koje definira maksimalne razlike u veličini atoma (< 15 %), kristalnoj stukturi, valenciji i elektronegativnosti. No ovdje je riječ o razlici veličine atoma od 42 % jer je radijus najmanjeg atoma, atoma kobalta jednak 126, a najvećeg atoma, atoma kositra 217 pm. Usto metali koji čine leguru 15-HEA kristaliziraju u četiri vrste kristalnih rešetki! Pa ipak, zahvaljujući „visokoentropijskom dizajnu“ (high-entropy design) ili „entropijom vođenom miješanju“ (entropic-driven mixing) autori spomenutog rada uspjeli su svih 15 vrsta atoma zgurati u jednu kristalnu rešetku, plošno centriranu kocku (FCC, face-centered cubic) sa stranicama od 378 pm.
Ako im je uspjelo napravili slitinu od 15 vrlo nesličnih metala, jasno je da je ovom novom metodom moguće dobiti praktički svaku slitinu. To nije mali uspjeh kada se zna da je dosad teoretski bilo moguće načiniti samo 200 slitina sa pet prijelaznih metala, dok je broj takvih kombinacija veći od stotinu tisuća (>105). Otvara se novo područje metalurgije, ali ne metalurgije kojom se bave metalurzi.

Riječ je o tome da se „visokoentropijskim dizajnom“ dobivaju nanočestice, a od nanočestica se očito ne mogu izrađivati zakovice i vijci, a ponajmanje avioni i brodovi. Njihova je namjena da budu katalizatori, a na katalizi i katalizatorima se temelji cijela kemijska industrija. No ne samo to. Iznađe li se dobar katalizator, skupu bi platinu u vodikovim ćelijama mogla zamijeniti slitina sastavljena od jeftinih metala. Novi katalizatori vodili bi i do novih vrsta akumulatorskih baterija, efikasnijih metoda elektrolize, novih metoda za pretvaranje ugljikova dioksida u metan i druge korisne organske spojeve, itd., itd. (Tehno)fantazija? Ne, nego gola činjenica – jer riječ je o milijunima novih, „nemogućih“ legura.

Nenad Raos je kemičar, doktor prirodnih znanosti i znanstveni savjetnik u trajnome zvanju, sada u mirovini. Autor je i koautor više od stotinu znanstvenih i stručnih radova iz područja bioanorganske i teorijske kemije, molekularnog modeliranja te povijesti kemije i komunikacijskih vještina u znanosti. Još od studentskih dana bavi se popularizacijom znanosti. Sada piše za Čovjek i svemir te, naravno, BUG online. Sedam je godina bio glavni i tehnički urednik časopisa Priroda, a danas je urednik rubrike Kemija u nastavi u časopisu Kemija u industriji. Koautor je dva sveučilišna udžbenika i autor 13 znanstveno-popularnih knjiga. Nagrađen je Državnom godišnjom nagradom za promidžbu i popularizaciju znanosti 2003. godine.























