Cijeljenje otvorenih kožnih ozljeda bez kirurgije i ožiljka
Znanstvenici su razvili metodu cijeljenja koja čak i duboke, upaljene otvorene rane zatvara prirodno, zamjenjujući ozlijeđeno i upaljeno tkivo normalnom kožom bez kirurških zahvata i bez ožiljaka
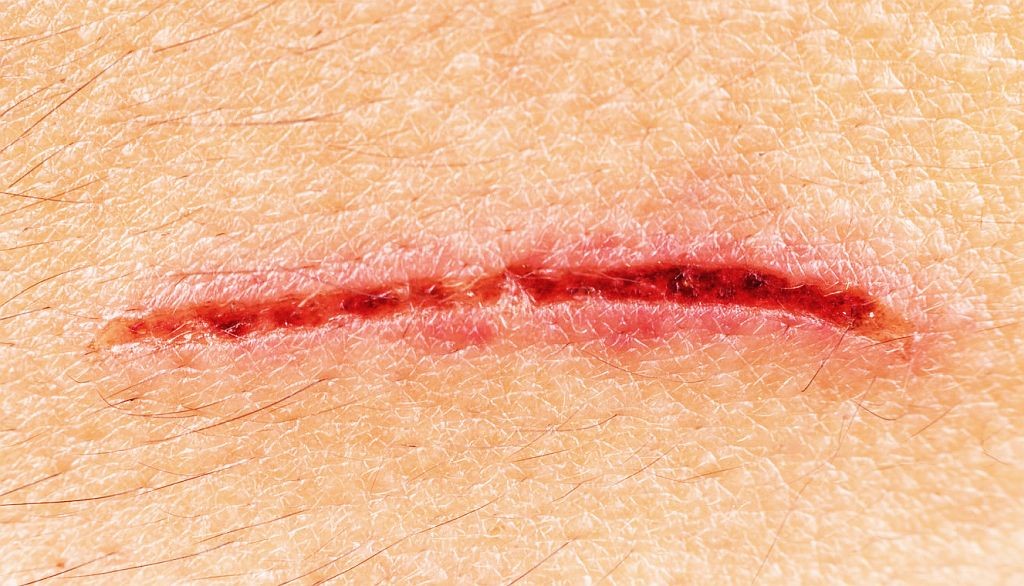
Iz osobnog iskustva znamo, a znanost i medicinska praksa to potvrđuju: plitke površinske rane koje se ne iskompliciraju upalom najčešće zarastaju bez ožiljaka, a veće i dublje rane nakon zarastanja za sobom ostavljaju ožiljak koji je nerijetko estetski i funkcionalno ružna uspomena na ozljedu.
Pluripotentni bazalni keratinociti
Ožiljno tkivo je većinom građeno od veziva koje posjeduje veću čvrstoću i manju elastičnost od normalnog površnog sloja kože (epidermisa). U normalnom procesu zarastanja (ciljeljenja) manjih ozljeda koje nisu komplicirane upalom i slabijom prokrvljenošću, presudnu ulogu imaju kožne stanice po imenu nediferencirani (bazalni) keratinociti, koji iz okolne neoštećene kože migriraju u rubove ozljeđenog dijela i tako ga postupno zatvaraju preciznim i finim procesom cijeljenja bez posljedičnog stvaranja ožiljka. Po nekim svojim svojstvima bazalni keratinociti se ponašaju kao matične stanice: posjeduju pluripotentnost, potencijal za pretvaranje u druge vrste kožnih stanica.
Međutim, bazalni keratinociti su odsutni u dubljim, težim ozljedama i ranama koje su izložene procesima upale i imaju lošu vaskularizaciju (dovod oksigenirane krvi). Takve rane zarastaju drugačijim procesom cijeljenja, u kojem se unutar rane ubrzano i masovno umnožavaju mezenhimalne stanice, čija primarna svrha nije (kao kod keratinocita) pravilno zatvaranje vanjskog sloja kože, nego one obavljaju robusniji, manje profinjen zadatak: pokretanje jakog i brzog lokalnog upalnog odgovora na ozljedu, kako bi se šupljina rane što prije popunila vezivnim tkivom i zatvorila.

S obzirom da su bazalni keratinociti matične, nediferencirane stanice, imaju potencijal diferencirati se u nekoliko tipova zrelih kožnih stanica. Postupci takvog pretvaranja jednih vrsta stanica u druge već su duže vrijeme standardni dio laboratorijskih procedura: iz tijela se uzme uzorak tkiva ili krvi iz kojega se izdvoje matične stanice, te ih se u laboratoriju podvrgne postupcima koji ih iz nezrelog, nediferenciranog oblika „usmjere“ prema sazrijevanju u željenu vrstu zrelih, formiranih stanica i tkiva.
Reprogramiranje mezenhimalnih stanica
No, znanost ne bi bila što jeste, da ne uspijeva iznova izmijeniti ustaljene paradigme: istraživački tim sa Salkovog instituta uspio je „redizajnirati“ mezenhimalne stanice i pretvoriti ih u bazalne keratinocite, ali bez angažiranja laboratorijskog okružja, tj. bez izdvajanja mezenhimalnih stanica iz organizma. Jednostavno rečeno: obavili su cijeli postupak unutar samog organizma.
Kako bi uspjeli u svojoj nakani da snažne i energične mezenhimalne stanice preobraze u profinjene, precizne keratinocite, proučavali su molekule koje igraju važnu ulogu u programiranju matičnih stanica kože i njihovom diferenciranju u zrele stanice svih slojeva kože. Od 55 potencijalnih molekularnih kandidata, naposlijetku su identificirali 4 proteinske molekule koje imaju glavnu ulogu u reprogramiranju zrelih mezenhimalnih stanica u nezrele keratinocite. Potom su tim proteinima tretirali laboratorijske miševe koji su imali kronične ulcerozne promjene kože (narodski rečeno: otvorene rane), nalik onima kakve imaju npr. dijabetičari i pacijenti s cirkulacijskim smetnjama na potkoljenicama ili nepokretne osobe koje imaju kronične rane od ležanja (dekubitus).

Za osamnaest dana od početka terapije reprogramirajućim proteinima, kožni ulkusi miševa zarasli su i prekrili se zdravom kožom. Stanice sa dna ulkusa ubrzano su se umnožile i potom praktički neprimjetno srasle i spojile se s okolnom kožom – čak i kada se radilo o značajno velikim i dubokim ranama. Prilikom testiranja nakon tri i šest mjeseci od zarastanja ulkusa, utvrđeno je da su novostvorene stanice vanjskim izgledom, karakteristikama i mikroskopskim svojstvima bile na staničnoj razini posve jednake okolnoj koži, a ne tvrdom i neelastičnom ožiljnom tkivu kakvo se inače stvara na mjestima zarastanja tako velikih ulkusa (ukoliko uopće zarastu).
Široka lepeza potencijalnih mogućnosti
Istraživači sada planiraju sljedeći korake u usavršavanje tehnike reprogramiranja mezenhimalnih stanica u keratinocite uz provođenje laboratorijskih tesatova na još različitih pokusnih modela ulkusa. Poboljšanje tehnologije staničnog reprogramiranja od velike je koristi i u boljem razumijevanju nastanka, razvoja i liječenja karcinoma kože, a može se iskoristiti i za unapređivanje konzervativnih (nekirurških) postupaka za oporavak svih vrsta kožnih ozljeda, kao i u kozmetologiji – za neutraliziranje vidljivih posljedica starenja kože.
Posebna korist od mezenhimalnog reprogramiranja očekuje se kod liječenja kožnih opeklina na većim površinama tijela, te u terapiji kroničnih rana koje teško zacjeljuju, kao što su kožni ulkusi dijabetičara ili duboke, inficirane dekubitalne rane ležećih pacijenata. Takvi kronični ulkusi koje dodatno pogoršava i loša cirkulacija, zahvaćaju duboko kroz sve slojeve kože, dosežući do mišića i kostiju, pri čemu predstavljaju mjesta za nastanak upornih i teško izlječivih infekcija koje za posljedice mogu imati razvoj općeg upalnog odgovora cijelog organizma (sepse), te dovesti i do potrebe za amputacijom ekstremiteta na kojima se takvu ulkusi razvijaju.

Od kirurgije do reprogramiranja
Do sada se terapija manjih kroničnih ulkusa sastojala u kirurškom zahvatu kojim su s rubova i dna ulkusa prvo odstranjivani odumrli slojevi tkiva, a potom se ulkus prekrivao transplantatom kože, najčešće uzetim od samog pacijenta sa zdravih dijelova tijela. Međutim, u slučajevima kada su ulkusi duboki, veliki i brojni, za transplantaciju treba uzimati vrlo velike dijelove zdrave kože, pa se zadnjih godina pribjegavalo tehnici laboratorijskog uzgajanja pacijentove kože od njegovih matičnih stanica.
Ali, takvi su postupci tehnički zahtjevni, skupi, nerijetko rizični za pacijenta, traže puno vremena potrebnog za uzgoj matičnih stanica i njihov rast do dimenzija dovoljnih za prekrivanje oštećenih dijelova kože. Povrh svega imaju relativno nizak postotak uspješnosti. Stoga se velike nade polažu u daljnji razvoj tehnika reprogramiranja matičnih stanica, njihov prelazak iz laboratorijskih u kliničke faze i početak njihove uspješne primjene kod ljudi.

Igor „Doc“ Berecki je pedijatar-intenzivist na Odjelu intenzivnog liječenja djece Klinike za pedijatriju KBC Osijek. Od posla se opušta antistresnim aktivnostima: od pisanja svojevremeno popularnih tekstova i ilustracija u tiskanom izdanju časopisa BUG, crtkanja grafika i dizajna, zbrinjavanja pasa i mačaka, fejsbučkog blogiranja o životnim neistinama i medicinskim trivijama, sve do kuhanja upitno pitkih craft-piva i posve probavljivih jela, te sviranja slabo probavljivog bluesa.






















