Trovanje živom: selenij je rješenje
Intoksikacija živom je vezivanje za sumpor, a detoksikacija vezivanje za selenij – najkraći je opis biokemije žive. I još: organizam se od tog otrova brani aminokiselinom koja se zove selenocistein.

Priča meni majstor, zidar koji je došao da mi pregradi kuhinju, kako se lijepo proveo kad je dobio posao u Sloveniji, u topionici žive pokraj Idrije. Prvo je trebao prenijeti boce od dvije litre. Dvije litre? Pa to se može podići sa dva prsta, pomislio je moj zidar, i mislio tako sve dok nije uhvatio bocu: dvije litre žive teži koliko i 27 litara vode! Živa je uz brom jedini tekući kemijski element, a gustoćom (13,5 g cm-3) premašuje olovo (11,3 g cm-3), što znači da olovo na živi pliva. Potom je trebao popraviti unutrašnju oblogu peći u kojoj je bila živa. I baš se htio prihvatiti posla, kad ugleda nekog radnika kako kako se sav trese. „Što je ovome?“, pita. To je jedan, rekoše mu, što je radio ono što ti trebaš raditi, pa se otrovao živom. Moj zidar odmah odjuri u kadrovsku službu da mu vrate radnu knjižicu. „Ali taj (što se trese) nije poštivao HTZ propise, nije nosio zaštitnu masku!“, pokušaše ga odgovoriti od njegova nauma, a on njima: „K vragu i maska i HTZ propisi, nećete me dobiti da se otrujem!“
I imao je na svoj način pravo. Živa je jak otrov o kojem bi se mnoge ovakve, i još mnogo gore priče mogle ispričati (njih ćete naći u mojoj knjizi „Metali života – metali smrti“), pa se u novije doba sve više izbjegava. Nitko više ne čuje ni za živine termometre, ni za živine barometre, a živini ispravljači električne struje mogu se vidjeti samo u muzeju. No živa je i čudan kemijski element. „Kad priređujem nove živine spojeve“, reče mi neka kemičarka, „nikad ne znam što ću dobiti, za što će se živa vezati“. I doista, živa se može za sve i svašta vezati, no najlakše se veže za sumpor.
Zato je i ekotoksikologija žive vrlo složena. U zraku se nalazi ponajviše u obliku para slobodne, elementarne žive (Hg0), u vodi u obliku iona Hg2+ i Hg22+ te u obliku čestica i taloga, netopljivih soli tih iona. No najopasnija je živa kada se, radom bakterija, pretvori u metilživu, (CH3)2Hg ili, kraće napisano, Me2Hg. Zbog lipofilnosti metilživa lako ulazi u masna tkiva morskih životinja pa onda truje i njih i sve one koji se njima hrane. Pa ipak, živi organizmi imaju način da se od tog otrova sami obrane. Kako? Na to su pitanje nedavno odgovorila osamnaestorica znanstvenika iz Francuske, Ujedinjenog Kraljevstva, Sjedinjenih Država i Brazila.

U znanstvenom radu „Demethylation of methylmercury in bird, fish, and earthworm (Dimetilacija metilžive u pticama, ribama i gujavicama)“, objavljenom u časopisu Environmental Science & Technology, objasnili kako se organizam rješava žive što je prima u obliku metilžive. (Udio žive u istraživanim uzrocima kretao se od 1,2 do 43 mg/kg). Metilživa se veže za atom sumpora aminokiseline cisteina, HSCH2CH(NH2)COOH (Cys). Tako nastaje kompleks MeHgCys koji raznosi živu po tijelu što joj omogućuje da se veže za spojeve sumpora, čime se, jasno, remete fiziološki procesi. To bi bio, jednostavno rečeno, mehanizam trovanja, intoksikacije. A što je s uklanjanjem otrova, detoksikacijom?
Za to postoji poseban protein, selenoprotein P (SelP). U njemu se nalazi aminokiselina koju nećete naći među 20 aminokiselina koje izgrađuju proteine. Ime joj je selenocistein, a kratica Sec ili U. A formula? HSeCH2CH(NH2)COOH. To je cistein kojemu je atom sumpora zamijenjen atomom selenija.
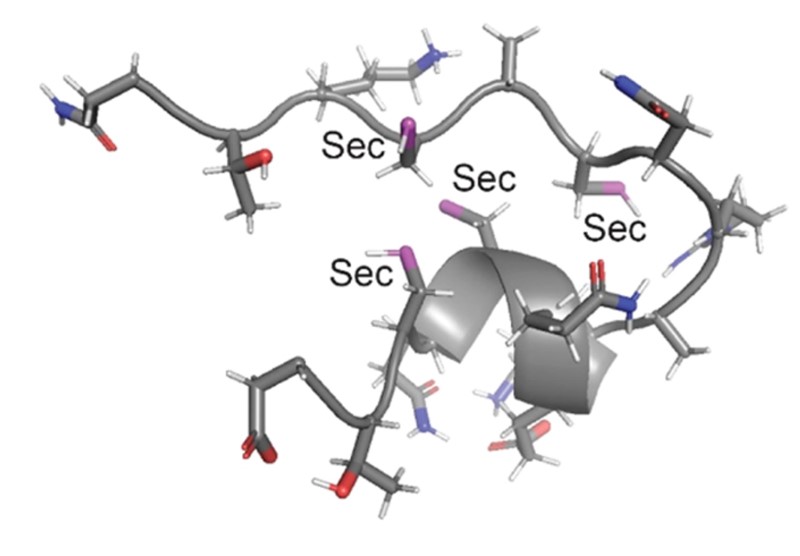
I što sad? Metilživa se veže za SelP, gubeći pritom metilnu skupinu, pa s njime gradi kompleks u kojem je atom žive okružen s četiri atoma selenija, ili – točnije – s četiri selenocisteinska ostatka, Hg(Sec)4. To se vezivanje događa na samom kraju molekule i to tako da se na svakom vrhu tetraedra nalazi jedan atom Se. Kao da se priroda pritom za sve pobrinula, jer upravo takvo vezivanje omogućuje redoslijed povezivanja amonokiselina u molekuli SelP, ...XUXUX6UXUX, gdje U označava selenocisteinski, a X bilo koji drugi aminokiselinski ostatak. Od tog proteina nastaju potom, još nedovoljno istraženim mehanizmom, čestice živina selenida, HgSe, koje se izlučuju bubrezima.
I što na kraju reći? Treba jesti hranu bogatu selenijem jer ćemo tako omogućiti organizmu ne samo da sintetizira dovoljne količine SelP za vezivanje žive nego i da nadoknadi selenij koji se izlučio u obliku HgSe. Priroda ima za sve rješenje, pa i za trovanje živom. Na nama je da joj u tome pomognemo.

Nenad Raos je kemičar, doktor prirodnih znanosti i znanstveni savjetnik u trajnome zvanju, sada u mirovini. Autor je i koautor više od stotinu znanstvenih i stručnih radova iz područja bioanorganske i teorijske kemije, molekularnog modeliranja te povijesti kemije i komunikacijskih vještina u znanosti. Još od studentskih dana bavi se popularizacijom znanosti. Sada piše za Čovjek i svemir te, naravno, BUG online. Sedam je godina bio glavni i tehnički urednik časopisa Priroda, a danas je urednik rubrike Kemija u nastavi u časopisu Kemija u industriji. Koautor je dva sveučilišna udžbenika i autor 13 znanstveno-popularnih knjiga. Nagrađen je Državnom godišnjom nagradom za promidžbu i popularizaciju znanosti 2003. godine.















