Kako (i koliko) munje čiste zrak
Poslije oluje čist je zrak, kaže narodna poslovica. To je sada egzaktno (i nemetaforički) dokazano zahvaljujući preciznim mjerenjima kemijskog sastava atmosfere i računalnim simulacijama.

„Prema tome možemo tvrditi da svaki iz puške ispaljeni hitac ubija, dapače da on uništava jednako mnogo života pogodilo tane živo biće ili ne“, pisao je krajem 19. stoljeća njemački fiziolog Gustav von Bunge, da bi potom to obrazložio: „Jer smrću jednog individua ne razara se život; iz tijela koje se raspada raste isto toliko novog života. Raspada li se pak vezani dušik, to se umanjuje definitivno ovaj kapital o veličini kojega ovisi suma života na Zemlji“. Ovaj Bungeov neočekivani zaključak ima opet veze s pokusom Stanleya Millera iz 1953. godine kojim je pokazao da su u prvotnoj Zemljinoj atmosferi mogle nastati aminokiseline i mnogi drugi za budući život važni kemijski spojevi. Kako? Kakve veze ima čudna tvrdnja njemačkog fiziologa s pokusom američkog kemičara koji je živio pola stoljeća poslije njega? Ima veze, ima – ta se veza zove munja.
Bunge je polazio od pretpostavke (bolje rečeno vjerovanja iz neznanja) da u prirodi ne postoje procesi koji bi stvarali „vezani dušik“, tj. dušikove spojeve iz atmosferskog, elementarnog („slobodnog“) dušika (N2), pa stoga biljke mogu crpiti dušik samo iz tla. Danas znamo da to nije istina. Biljke mogu uzimati dušik i iz zraka zahvaljujući simbiozi s mikrobima (zelena gnojidba). No ima još jedan proces. Dušikovi oksidi, a od njih nitrati, stvaraju se i u zraku djelovanjem električnog pražnjenja, sijevanjem munja. Na toj je pretpostavci mladi američki kemičar Stanley Miller osmislio svoj pokus, jer je energiju za sintezu aminokiselina i drugih organskih spojeva davalo upravo električno pražnjenje, kojim je oponašao sijevanje munja u pradavnoj atmosferi našeg planata.
Da prolazak električne iskre kroz zrak izaziva mnoge kemijske reakcije, u kojima na kraju nastaju dušikovi oksidi (označeni kao NOx), a još više ozon (O3), zna se poodavno. (Ne samo da se zna, nego se iskrenje koristi za dobivanje ozona, a nekoć se koristilo i za proizvodnju dušične kiseline.) No ono što se nije znalo je koliko se čega stvara pri sijevanju munja i, još više, koliki je ukupni sintetički potencijal Zemljine atmosfere.
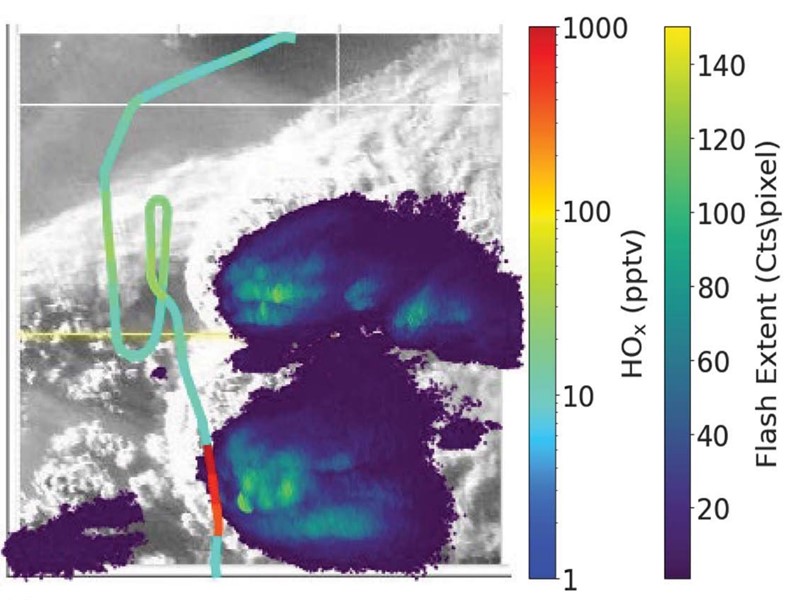
To se saznalo tek nedavno, točnije koliko-toliko precizan proračun o tome objavljen je u svibanjskom broju časopisa Science pod naslovom „Extreme oxidant amounts produced by lightning in storm clouds (Ekstremne količine oksidansa proizvedene sijevanjem munja u olujnim oblacima)“. Još čudnije, znanstveni rad desetorice američkih znanstvenika temelji se na mjerenjima koja su obavljena još 2012. godine.

U ljetu 2012. godine američki su znanstvenici letjeli avionom kroz olujne oblake te u njima mjerili koncentracije 200 sastojaka, a prije svega koncentracije slobodnih radikala HO i HO2 (označenih kao HOx), dušikovih oksida NO i NO2 (NOx) te ozona (O3). Sve su to vrlo reaktivne molekulske vrste: NOx živi u atmosferi tek nekoliko sati, a HOx samo nekoliko minuta. Gdje da počnem? Sijevanje munje izaziva disocijaciju molekula vode na radikale H, HO i HO2. HO2 reagira sa NO dajući NO2 i HO. NO2 se potom razlaže Sunčevim zračenjem dajući ozon ili pak reagira s vodom dajuću dušičnu kiselinu (koja gnoji zemlju). Itd., itd. No u svem tom metežu molekula i reakcija, ističu se dvije ključne i najreaktivnije molekulske vrste, najreaktivniji radikali, HO i HO2. Koliko ih nastaje pri sijevanju munje?
Odgovor se krije u naslovu, u izrazu „extreme oxidant amounts“. Mjerenja su pokazala da udjel HOx u zraku raste nakon sijevanja munje ispred aviona od 5 – 20 na 700 – 2000 pptv (1 pptv = 0,001 ppb; v = volumni udjel). Drugim riječima, oluja stvara u sekundi između 3,1·1025 i 2,5·1026 molekula OH (rezultat ovisi o računalskoj metodi).
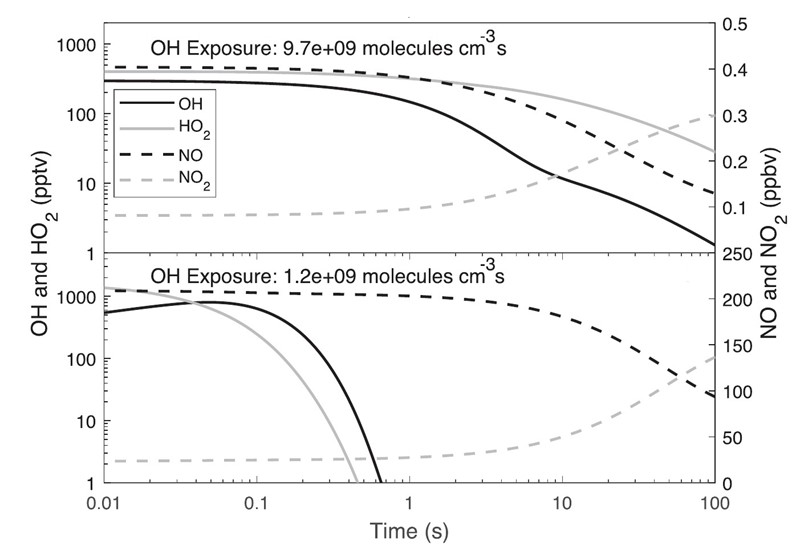
Bez obzira na veliku neodređenost, riječ je o velikim brojevima, posebice kada se pomnože sa 1800 oluja koje istodobno bjesne na Zemlji. Rezultat je 5,6·1028 (4,9·1029) molekula HO, a to znači 1,6 (14) tona – svake sekunde.
Rezultat je neočekivan jer to znači da 2 – 16 % oksidacijskog potencijala atmosfere potječe od munja i oluja. Ili, jednostavnije rečeno, munje sudjeluju 2 – 16 % u čišćenju zraka od plinova koji mu izvorno ne pripadaju, uključujući i one stakleničke poput metana i kloriranih ugljikovodika. No te zaključke ostavimo znanstvenicima koji se bave atmosferskim procesima i kemičarima koji istražuju reakcije radikala u plinskoj fazi, a mi se zadovoljimo time da znamo zašto je zrak nakon oluje čist.

Nenad Raos, rođen 1951. u Zagrebu, je doktor prirodnih znanosti iz područja kemije, znanstveni savjetnik u trajnome zvanju. Do umirovljenja radio je u zagrebačkom Institutu za medicinska istraživanja i medicinu rada (IMI) baveći se bioanorganskom i teorijskom (računalnom) kemijom. Još od studentskih dana bavi se popularizacijom znanosti. Napisao je više od dvije tisuće znanstveno-popularnih članaka, 13 znanstveno-popularnih knjiga te u koautorstvu dva sveučilišna udžbenika iz područja dizajniranja lijekova. U časopisu Kemija u industriji je stalni komentator te urednik rubrike „Kemija u nastavi“. Godine 2003. dodijeljena mu je Državna godišnja nagrada za promidžbu i popularizaciju znanosti.




























