Iz kineskog laboratorija: svila čvršća od svile
Kako otopiti pamuk, a zatim iz otopine izvući čvršću celuloznu nit znali su kemičari još u 19. stoljeću. Može li se to napravi i sa svilom, s proteinskim vlaknom? Može – ali tek u 21. stoljeću.

Zašto u našem dalmatinskom primorju i, još dublje, u dalmatinskoj zagori posvuda vidimo dudovo drvo iliti murvu po vlaški? Od dudova ploda malo koristi, od dudova se drva – kažu – mogu raditi dobre bačve za rakiju, i ništa više. Ništa više? Dud je u Dalmaciju došao s francuskom upravom jer je nova vlast htjela u pasivnim krajevima razviti svilarstvo, a dudov svilac, samo ime kaže, živi na dudu gdje se hrani njegovim lišćem. No list se s duda može ubrati i staviti u kutiju s ličinkama, a kada se ličinke začahure onda se stave u vrelu vodu da bi se potom od njihove kukuljice napravila svila. Kako? Naše se prabake i šukunbake na hrvatskom jugu nisu suviše mučile tehnologijom svile nego su je prele kao vunu. Pričao mi je moj otac kako mu je majka isplela od prst debele svile „bičve“ koje je nosio za cijelog školovanja u Splitu – i nije ih poderao.
No pustimo sad transfer tehnologije, tehnološke inovacije i improvizacije. Ono što prede dudov svilac (Bombyx mori) samo je jedna svilena nit od koje isprede čitavu kukuljicu. Onaj tko hoće presti svilu mora naći početak te niti i potom je odmotati od kukuljice kao od vretena. To je vještina svilarskog zanata, no što je svila kemijski?
Najvažniji sastojak svile (svilenog vlakna) je fibroin. Iza tog imena krije se protein, točnije polipeptidni lanac sekvencije -Gly-Ser-Gly-Ala-Gly-Ala-. Veliki sadržaj, 50 %, glicina (Gly) daje svili čvrstoću jer molekule glicina nemaju pobočnih lanaca koji bi sprječavale molekule fibroina da se čvršće pakiraju, sa što manje praznine među njima. Druge dvije molekule, alanin (Ala) i serin (Ser), imaju doduše pobočne lance, no oni su najkraći među molekulama aminokiselina: pobočni lanac alanina je -CH3, a serina -CH2OH. Priroda je došla do savršenstva. Da li baš?
Od svilene niti još je čvršća nit paučine, koja je usto skoro četiri puta tanja i gotovo isto toliko čvršća od svilene niti: prekidna čvrstoća svile iznosi 400 – 600 MPa, a paukove niti 0,9 – 1,4 GPa. I tu bi priči bio kraj.

No istraživanju nikad kraja nema. Tome svjedoči članak kineskih znanstvenika objavljen u časopisu Matter: „Artificial superstrong silkworm silk surpasses natural spider silks“. Napravili su od svile (silkworm silk) paučinu (spider silk)?
Njihova metoda, mogli bismo tako reći, je stara gotovo dva stoljeća samo je primijenjena na drugu vrstu vlakna. Jer kao što su europski kemičari uspjeli dobiti regeneriranu celulozu (viskozu) u 19. stoljeću, tako su se kineski kemičari u 21. stoljeću potrudili da to isto učine sa svilom.
Postupak je sasvim jednostavan. Sirovu su svilu, nakon čišćenja od voska i drugih neželjenih sastojaka, otopili u koncentriranoj otopini (9,8 mol/L) litijeva bromida (LiBr) zaluženu sodom (natrijevim karbonatom). Svila, točnije fibroin, u toj se otopini potpuno otopio. Kako iz nje opet dobiti svilu? Starom metodom: u otopinu su dodali amonijev sulfat – poznato sredstvo za taloženje („isoljavanje“) proteina – uz još jedan važan dodatak: cinkov sulfat.
Cinkovi su ioni (Zn2+) učinili čudo, jer su omogućili bolje povezivanje fibroinskih lanaca. Cink ima naime veliki afinitet prema kisiku, pa kad se nađe u blizini dviju hidroksilnih skupina veže se za njih – i tako povezuje molekule fibroina u čvrstu mrežu. Hidroksilne skupine nalaze se, kao što sam već spomenuo, u molekulama serina, a serina u svili ima 12 %.
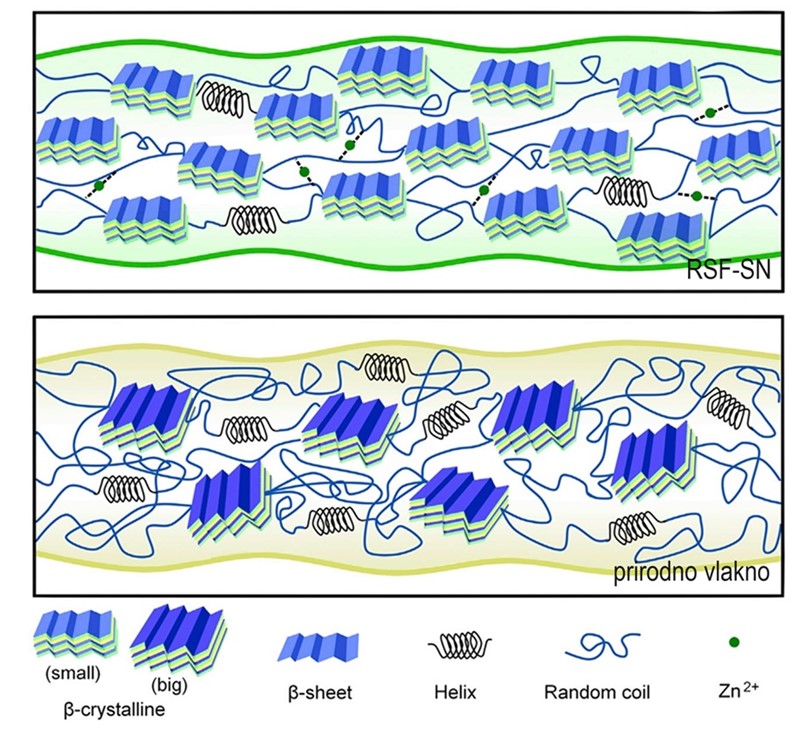
No to nije sve, jer regenerirana svila ima i bolju strukturu. Da bismo razumjeli što to znači, treba znati da polipepidni lanac nije ispružen, nego na neki način namotan. Kemičari razlikuju tri osnovna načina „namatanja“ proteinskog lanca. Prvi je namot posve nasumičan (random coil). Druga su pak dva namota pravilna. Prvi namot je zavojnica ili, točnije, alfa-zavojnica (α-helix). No za razliku od molekula DNA koje grade dvostruku zavojnicu, α-zavojnica proteina je jednostruka te – kao i zavojnica DNA – sasvim pravilna: u svakom zavoju nalazi se točno 3,6 aminokiselinskih ostataka. No ta struktura ne pridonosi čvrstoći proteina, pa tako ni fibroina. Njegovoj čvrstoći pridonose plosnate strukture, beta-ploče (β-sheets) jer su kompaktnije, a osim toga se slažu jedna na drugu i tako učvršćuju lanac. Da je upravo to uzrok povećanja čvrstoće svile nakon regeneracije pokazala su mjerenja: udio beta-ploča porastao je od 44,2 na 55,8 %, a nasumičnog klupka opao sa 22,1 na 14,8 %.

Konačan rezultat: prekidna čvrstoća svile povećala se na 2,0 GPa, uz Youngov modul elastičnosti na 43 GPa, čime je regenerirana svila kineskih znanstvenika nadmašila za 60 – 70 % najčvršću prirodnu nit – vlakno paučine (dragline).

Nenad Raos je kemičar, znanstveni savjetnik u trajnome zvanju, koji je radio do umirovljenja 2016. godine u zagrebačkom Institutu za medicinska istraživanja i medicinu rada (IMI). Autor je i koautor oko 200 znanstvenih i stručnih radova iz područja teorijske (računalne) kemije, kemije kompleksnih spojeva, bioanorganske kemije, povijesti kemije i komunikacijskih vještina u znanosti. Bio je pročelnik Sekcije za izobrazbu Hrvatskog kemijskog društva, glavni urednik Prirode te urednik rubrike Kemija u nastavi u časopisu Kemija u industriji; član je društva ProGeo-Hrvatska i Odjela za prirodoslovlje i matematiku Matice hrvatske. Još od studentskih dana bavi se popularizacijom znanosti. Autor je 15 znanstveno-popularnih knjiga, posljednje dvije su „Kemija – muza arhitekture“ (u koautorstvu sa Zvonkom Pađanom) i „Kemičar u kući – kemija svakodnevnog života“.















