Ostvaren veliki napredak u razvoju materijala za gorive ćelije
Oblaganjem nanočestica srebra polimerom, ionskim izmjenjivačem, dobiva se novi kompozitni materijal - i vrlo efikasan elektrokatalizator koji omogućuje izradu izuzetno jakih vodikovih ćelija
Električni se naboj, zna se, može prenositi na dva načina – elektronima i ionima. Elektroni se gibaju u čvrstim tvarima, kovinama, a ioni u tekućinama, elektrolitima. Uronimo li u vodenu otopinu natrijeva ili kalijeva hidroksida elektrode, elektroni koji su električnim vodom stigli do katode spojit će s vodikovim ionima, koji su do nje doputovali elektrolitom – te će nastati plinoviti, elementarni vodik, H2. (Druga pak elektroda, anoda, privlači hidroksidne ione. Oni otpuštaju elektrone i prelaze u elementarni kisik, O2). Obratno se događa u gorivnim ćelijama: vodik (u dodiru s anodom) i kisik (u dodiru s katodom) spajaju se u vodu i pritom nastaje električna struja, elektroni koji putuju žicom od anode do katode.
Prve upotrebljive gorivne ćelije malo su se razlikovale od opisanog uređaja za elektrolizu vode. Alkalne gorivne ćelije (alkaline fuel cells, AFC), razvijene za potrebe projekta Apollo (snage 1,4 kW) i Space Shuttle (12 kW), sadržavale su – samo im ime kaže – alkalni elektrolit (kalijevu lužinu). Radile su pri temperaturi od 60-120 oC, sa specifičnom snagom od 12,5 W/kg (Apollo), pa i 150 W/kg (Space Shuttle). I što dalje? Lužina se može zamijeniti otopinom fosforne kiseline (phosphoric acid fuel cells, PAFC) ili talinom smjese litijeva i kalijeva karbonata (molten carbonate fuel cells, MCFC) – no ove posljednje ćelije rade, razumije se, pri znatno višim temperaturama, naime 600 – 700 oC.
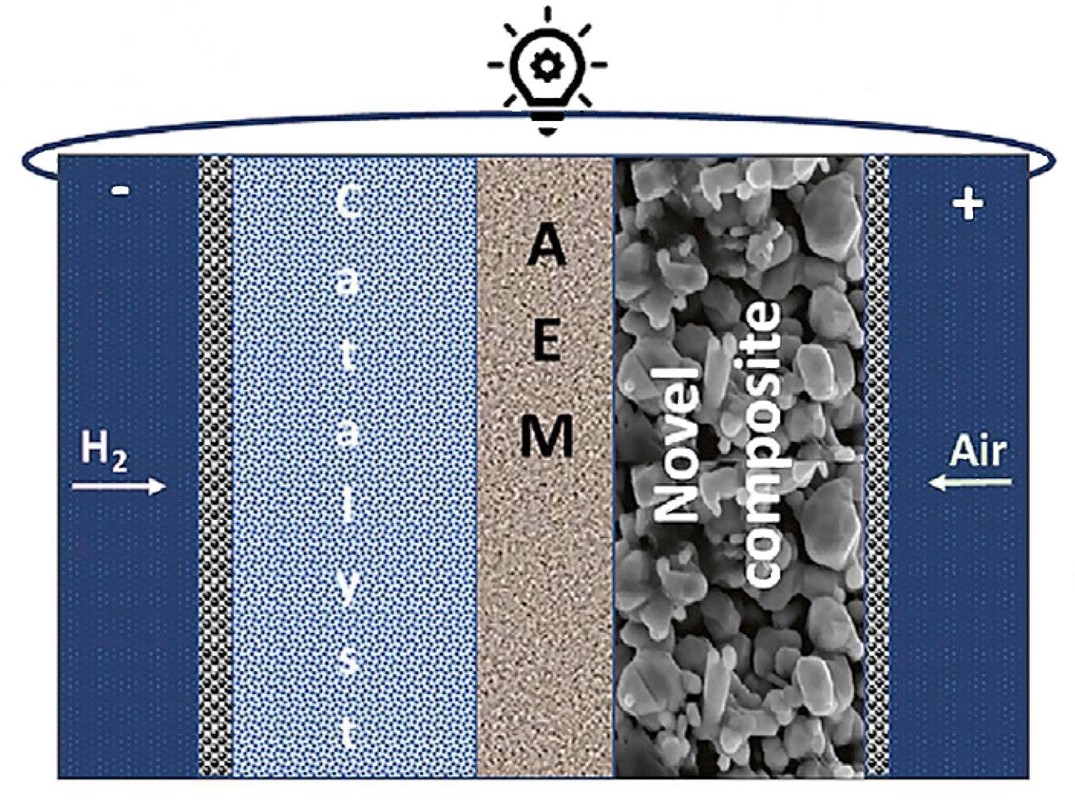
U gorivnim ćelijama moraju se odvijati tri procesa: vođenje elektrona, vođenje iona i katalitička reakcija elektrona s ionima i molekulama – jer bez katalizatora kisik se ne bi mogao spojiti s vodikom pri temperaturi nižoj od temperature paljenja (700 oC). Sva se ta tri procesa događaju u novom materijalu jednostavne oznake: ionomer@Ag (ili, određenije, FAA-3@Ag).

Riječ je o kompozitnom materijalu (ili materijalima) s kombiniranim elektronskim i ionskim svojstvima (composite materials with combined electronic and ionic properties), kako glasi naslov znanstvenoga rada međunarodne ekipe iz Sjedinjenih Država, Izraela, Njemačke i Ujedinjenog Kraljevstva objavljenog ove godine u časopisu Matter. Znanstvenici su vodič elektrona (srebro) i vodič iona (polimerna smola FAA-3) ujedinili u jednu česticu, nanočesticu FAA-3@Ag (oznaka @ znači da je čestica Ag obložena polimerom FAA-3). Nanočestice FAA-3@Ag, koje sadržavaju 91,7 % srebra i samo 8,3 % FAA-3 (no po volumenu 61,3 % Ag i 38,7 % FAA-3), potom se udružuju u agregate tvoreći tako poroznu tvar izuzetnih svojstava. Kako je polimer FAA-3 – derivat poli(fenilen-oksida) – anionski izmjenjivač velikog kapaciteta, novi kompozitni materijal gradi membranu koja izmjenjuje anione (anion-exchange membrane, AEM).

Ono što me fascinira u kemiji, a nevježi je teško razumjeti, je kako se s jako malo može postići jako mnogo. To se vidi i ovdje. Sasvim malo (8,3 %) ionomera više je nego deseterostruko poboljšalo svojstva gorivne ćelije. Dok srebrna katoda (kisikova elektroda) ima gustoću snage oko 12 mW cm-2 (120 W m-2), katoda temeljena na nanočesticama FAA-3@Ag može imati i 200 mW cm-2 (2 kW m-2). Slično je i s maksimalnom gustoćom jakosti struje: srebrna katoda daje oko 70 mA cm-2 (700 A m-2), a nova elektroda 800 mA cm-2 (8000 A m-2).
Autori o svome „kompozitnom materijalu s kombiniranim elektronskim i ionskim svojstvima“ misle, a što drugo nego sve najbolje. „Takvi materijali mogu imati bezbrojne primjene u mnogim elektrokemijskim uređajima, a ne samo u gorivnim ćelijama kako je ovdje prvi put pokazano“, kažu.
No kako bilo da bilo, pred gorivnim, vodikovim ćelijama je budućnost: nećemo dugo čekati da one počnu zamjenjivati litij-ionske baterije, posebice u velikim vozilima – kamionima, brodovima, podmornicama i avionima. Višak energije iz vjetroelektrana i drugih alternativnih izvora energije mogao bi se najjeftinije skladištiti u obliku vodika, a gorivne ćelije bi se – izravno ili neizravno – mogle napajati i drugim gorivima, primjerice metanom ili metanolom. No, to je već tema za drugi članak.

Nenad Raos, rođen 1951. u Zagrebu, je kemičar, doktor prirodnih znanosti i znanstveni savjetnik, sada u mirovini. Još od studentskih dana bavi se popularizacijom znanosti pišući za časopise Prirodu (kojoj je sedam godina bio i glavni urednik), Čovjek i svemir, ABC tehnike, Smib, Modru lastu, a u posljednje vrijeme i za mrežne stranice Zg-magazin te, naravno, BUG online. Autor je više stručnih i 13 znanstveno-popularnih knjiga, a upravo mu izlazi još jedna: „Mala škola pisanja (za znanstvenike i popularizatore)“. Urednik je rubrike „Kemija u nastavi“ u časopisu Kemija u industriji, za koji piše i redovite komentare. Nagrađen je Državnom godišnjom nagradom za promidžbu i popularizaciju znanosti 2003. godine.






























